- 飽和水蒸気圧(ほうわすいじょうきあつ)とは、空気中にそれ以上水蒸気を含むことができなくなる限界の水蒸気の圧力のこと。
- 表面張力(ひょうめんちょうりょく)とは、液体の表面が、まるで「薄い膜」のようにピンと張っている力のこと。
- 小さな水滴は、「蒸発しやすい」=「凝結しにくい」
受講生の方から、水滴に対する飽和水蒸気圧について質問です!

飽和水蒸気圧って、水滴の表面張力の影響で、水面に対する値より大きくなるのはなぜですか?
一見すると別々の現象に見える表面張力と飽和水蒸気圧ですが、実は密接な関係にあります。
例えば、非常に小さな水滴ほど蒸発しやすい、という現象をご存知でしょうか?
これは、水滴の曲率が表面張力と飽和水蒸気圧に影響を与え、その結果、蒸発のしやすさが変化・・・という解説よりも優しく!わかりやすく!簡潔に!を目指して解説していきます。
※この記事は、当講座に在籍する気象予報士が監修しております。
飽和水蒸気圧と表面張力の基本概念
まず・・・飽和水蒸気圧と表面張力について、しっかり理解できていないと話が進みません!
ここでしっかりおさらいしてから進みましょう!
飽和水蒸気圧とは?
飽和水蒸気圧(ほうわすいじょうきあつ)とは、空気中にそれ以上水蒸気を含むことができなくなる限界の水蒸気の圧力のこと。
空気には、水蒸気を含むことができますが、温度によって限界(=飽和)があります。
そのときの水蒸気がつくる圧力を「飽和水蒸気圧」と呼びます。
温度が高くなるほど、空気はたくさんの水蒸気を含めるので、飽和水蒸気圧も大きくなり
逆に、温度が低いと飽和水蒸気圧も小さくなります。
表面張力とは
表面張力(ひょうめんちょうりょく)とは、液体の表面が、まるで「薄い膜」のようにピンと張っている力のこと。
水などの液体では、分子どうしが引っ張り合う力(分子間力)があります。
液体の内部では、四方八方から引っ張られてバランスがとれていますが、表面にある分子は上から引っ張られないので、内側に引っ張られる力が働きます。
その結果、液体は表面積をできるだけ小さくしようとします。
たとえば水が「球状の水滴」になるのも、表面積を最小にする=表面張力の影響です。
この力のために、水滴がぷるっと丸くなったり、小さな虫が水に浮かんだりします。
気象では、小さな水滴ができにくく、蒸発しやすい(飽和水蒸気圧が高くなる)という点で大切な現象です。
水滴に対する飽和水蒸気圧
水滴に対する飽和水蒸気圧は、水面に対する値よりも大きくなります。
その理由は、主に水滴の表面張力による効果です。
詳しく説明すると、以下のようになります。
表面張力による内部圧力の増加
水滴は表面張力によって、表面積を最小にしようとする力が働いています。
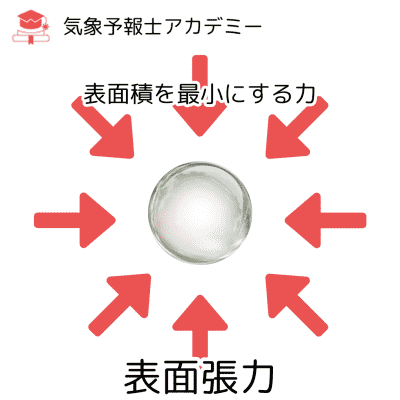
この力によって、水滴内部では、周囲の空気よりも強い圧力が発生します。
しかも小さい水滴ほど曲率が大きいため、水滴が小さければ小さいほど、内部圧力はより高くなります。
蒸発の促進
水滴内部の圧力が高くなると、水分子が水滴の表面から蒸発しようとする傾向が強まります。
要するに「蒸発しやすい」状態です。
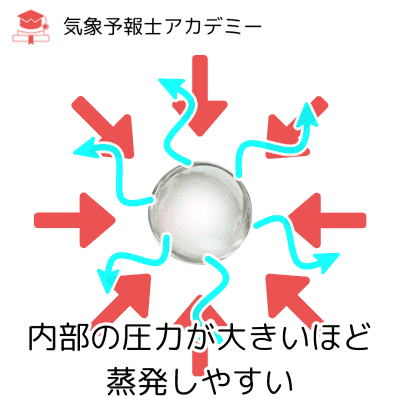
これは、高圧の環境では分子がより活発に運動し、液体表面から飛び出しやすくなるためです。
元気いっぱいで、水分子が水滴から飛び出したがっているイメージです。
平衡状態の変化
飽和水蒸気圧とは、蒸発と凝縮が平衡状態にあるときの水蒸気の圧力です。
水滴の場合、表面張力によって蒸発が促進されるため、平衡状態を保つためには、より高い水蒸気圧が必要となります。
つまり、水滴の周囲の空気中の水蒸気圧が、平らな水面の場合よりも高くないと、水滴は蒸発してしまうのです。
水滴の径(直径とか半径)が小さいほど表面張力が強くなり、
「水滴が壊れやすい=蒸発しやすい」となります。
用語整理
「飽和」=空気に限界まで水蒸気が含まれている状態です。
「飽和水蒸気圧」=空気が限界まで水蒸気を含んだときの水蒸気圧です。
さいごに
「小さな水滴」は
「蒸発しやすい」=「凝結しにくい」ということが言えます。
🔹 水面(広い水たまりなど)→ 表面張力の影響が小さい → 飽和水蒸気圧は低め
🔹 水滴(小さい)→ 表面張力の影響が大きい → 飽和水蒸気圧は高くなる
これは、雲粒のような小さな水滴が安定して存在しにくく、蒸発しやすい理由の1つでもあります。
気象予報士試験でも、度々関連した問題が出題されていますので、受験を予定されている方はしっかり理解しておくようにしましょう!
「気象予報士の資格は取りたいけど、どのように勉強すれば良いのかわからない」
「テキストを買ってみたけれど、わからないことだらけ…」
「一人で受験勉強をする自信がない」
などなど、一人で悩んでいませんか?
当講座では、この記事で解説したような専門的な内容も、初学者の方が基礎から着実に理解できるようカリキュラムを組んでいます。
AIチューターが即座に疑問を解消し、担当講師がマンツーマンで、あなたの『わからない』を徹底的にサポート。
勉強内容だけでなく、あなたに最適な学習計画も一緒に考え、独学では難しい最新の予報技術も効率的に習得できます。
今すぐ、気象予報士合格への第一歩を踏み出しませんか?
▶︎【合格ロードマップ公開!】気象予報士アカデミーで学ぶ最短合格への3ステップ
LINEで友達登録すると、3分でわかる気象予報士合格ポイント動画をプレゼント!
マンツーマンの受講相談で、あなたの疑問や不安を解消しましょう!!!
\ 講座へのご質問はお気軽に! /